ファイザー製ワクチン、3回目接種後の副反応は?
以下は、記事の抜粋です。
米国食品医薬品局(FDA)は9月22日、ファイザー/ビオンテック社製COVID-19ワクチン(BNT162b2)の3回目接種(ブースター接種)について、65歳以上や重症化リスクの高い人などを対象に緊急使用許可を承認した。この承認に当たりファイザー社が提出した資料の安全性データについて以下にまとめる。
対象:phase1試験から12人(65~85歳)、phase2/3試験から306人(18~55歳)
試験概要:参加者はBNT162b2 30μgの2回接種の後、phase1試験参加者は約7~9ヵ月後、phase2/3試験参加者は約6ヵ月後にBNT162b2 30μgの3回目接種を受けた。
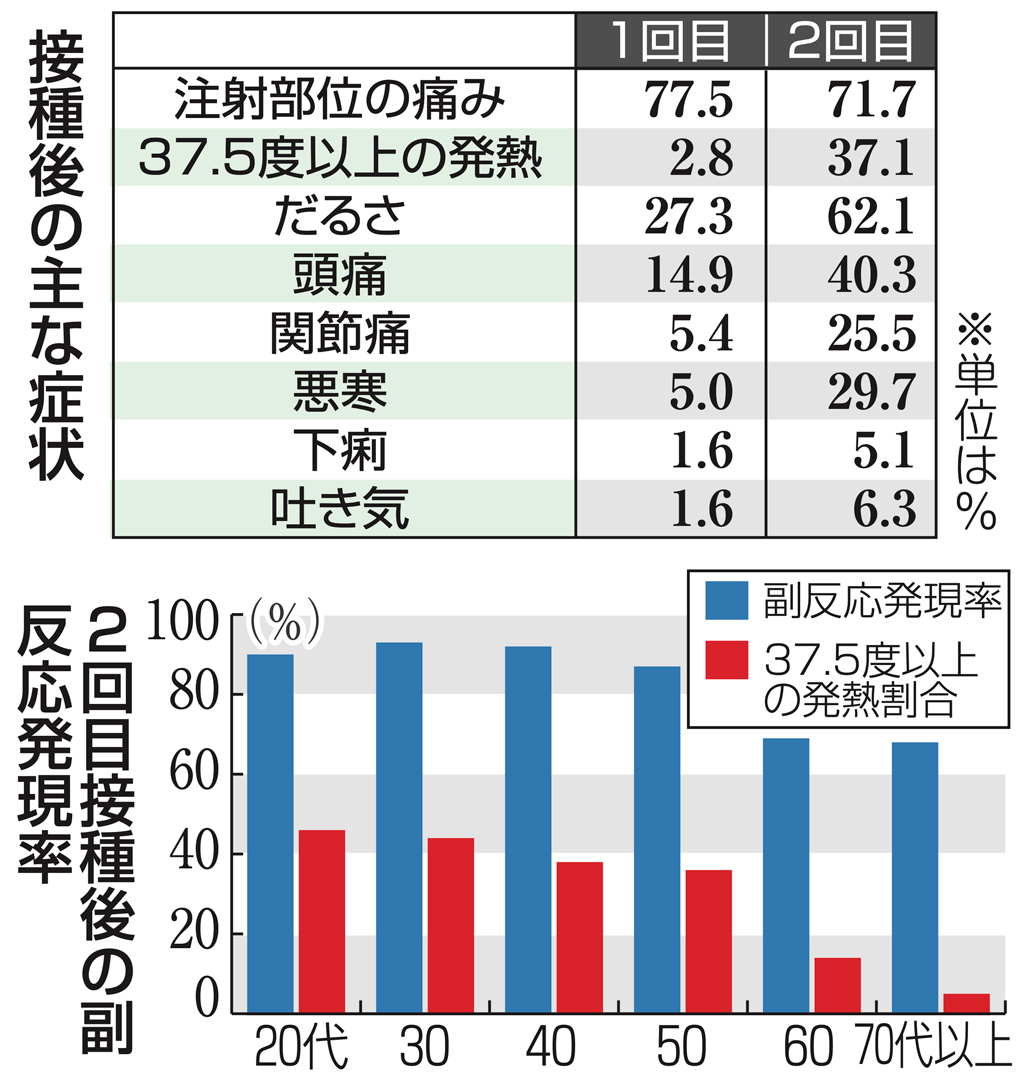
安全性の評価:参加者はブースター接種後1日~7日目まで副反応と解熱鎮痛薬の使用について報告した。副反応には、接種部位反応(痛み、発赤、腫れ)および全身性反応(発熱、倦怠感、頭痛、悪寒、吐き気、下痢、筋肉痛、関節痛)が含まれる。その他の安全性評価には、各投与後30分以内に発生する副反応、1回目投与からブースター接種後1ヵ月間の非重篤な未確認の副反応、およびブースター接種からデータカットオフ日までの重篤な副反応が含まれた。
1回目(dose1、16~55歳、2,899人)、2回目、dose216~55歳、2,682人)のデータと比較した3回目(dose3)接種後の副反応報告は以下のとおり。
接種部位反応
・痛み:dose1(83.7%)、2(78.3%)、3(18~55歳:83.0%、65~85歳:66.7%)
・腫れ:dose1(6.3%)、2(6.8%)、3(18~55歳:8.0%、65~85歳:0.0%)
・発赤:dose1(5.4%)、2(5.6%)、3(18~55歳:5.9%、65~85歳:0.0%)
全身性反応
・倦怠感:dose1(49.4%)、2(61.5%)、3(18~55歳:63.8%、65~85歳:41.7%)
・頭痛:dose1(43.5%)、2(54.0%)、3(18~55歳:48.4%、65~85歳:41.7%)
・筋肉痛:dose1(22.9%)、2(39.3%)、3(18~55歳:39.1%、65~85歳:33.3%)
・悪寒:dose1(16.5%)、2(37.8%)、3(18~55歳:29.1%、65~85歳:16.7%)
・関節痛:dose1(11.8%)、2(23.8%)、3(18~55歳:25.3%、65~85歳:16.7%)
・下痢:dose1(10.7%)、2(10.0%)、3(18~55歳:8.7%、65~85歳:0.0%)
・嘔吐:dose1(1.2%)、2(2.2%)、3(18~55歳:1.7%、65~85歳:0.0%)
・発熱(≧38.0℃):dose1(4.1%)、2(16.4%)、3(18~55歳:8.7%、65~85歳:0.0%)
・解熱鎮痛薬の使用:dose1(27.8%)、2(45.2%)、3(18~55歳:46.7%、65~85歳:33.3%)
報告書では、ブースター接種後に報告された副反応の頻度および重症度は、2回目接種後と差がみられなかったとしている。
2回目から6~9か月後に行った3回目接種の副反応は2回目とほぼ同じという結論です。発熱などは、3回目の方が少ないです。また、副反応は年齢が高くなると出にくい事がこのデータからも明かです。熱が出たら、若いと思いましょう。
モデルナ社のワクチンはファイザー社のものよりも副反応は強い傾向のようですが、おそらく同様の結果だと思います。怖がらずに3回目も受けましょう。

コメント