がん免疫療法の時代が到来
以下は、総説要約の抜粋です。
がんで免疫系を活性化して治療効果を上げることは、ずっと以前から免疫学と腫瘍学の目標であった。失望する結果が何十年も続いた後、最近の概念実証型(proof-of-concept)の臨床試験の成功により、ついに流れが変わった。
注目すべき結果は、抗CTLA4抗体であるイピリムマブ(ipilimumab)が、従来の治療法が無効であった転移性メラノーマ患者の生存期間を有意に延長したことである。
寛容、免疫、免疫抑制などのメカニズムが抗腫瘍免疫応答を調節する仕組みの解明が進むと同時に、分子標的療法が夜明けを迎えている状況の中、これらの成功は、能動的免疫療法ががん患者において、丈夫で長持ちする応答を得る手段であることを示唆している。
モノクローナル抗体(抗体医薬)やドナーT細胞を使う免疫療法が有効ながん治療法であることは、近年の多くの臨床試験によって確立されています。これらは、「受動的免疫療法」とよばれています。患者が自分で抗体をつくらず、できた抗体を投与されるからでしょう。
また、ヒトパピローマウィルスやB型肝炎ウィルスなどに対するワクチンが、子宮頸がんや肝がんの予防に効果があることも確立されています。これは能動的ですが、健常人に対して予防的に行なうものです。本総説の話題は、できてしまったがんに対する「能動的免疫療法」です。
本総説が特に強調しているのは、抗CTLA4抗体であるイピリムマブ(ipilimumab)の成功です。これは、T細胞の生物学の進歩、具体的にはT細胞の培養法や遺伝子導入法の確立に基づくT細胞制御因子の研究成果に基づくものです。分子標的となったcytotoxic T-lymphocyte-associated antigen 4 (CTLA4)は、多くのグループによって研究され、その機能が解明された最も重要なT細胞抑制因子の一つです。
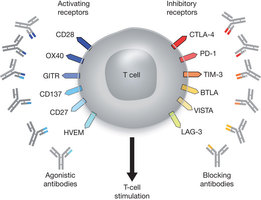
CTLA4などの抑制因子の機能を中和抗体で抑制すれば、非特異的な炎症などの副作用がおこることは当然ですが、末期メラノーマ患者への効果はこれらのデメリットを上回るものでした。今後は、下図に示したように、CTLA4以外のT細胞抑制因子や活性化因子を分子標的とする治療が開発されると思います。
一方、各種の菌やその抽出物、あるいはペプチドなどのがん特異抗原を腫瘍や患者に注射して抗腫瘍免疫力を高めるタイプの能動的免疫療法は、未だ大きな成功をみていません。ものすごい額の研究費(大半は税金)を使って研究し、その成果を持ってシカゴ大に移籍すると報道された中村祐輔氏の「がんワクチン」もこのタイプですし、作日紹介した「ニキビ菌ワクチン」もこのタイプです。
これらのがん特異抗原の認識には樹状細胞が重要であることがわかっています。今年のノーベル賞を受賞したラルフ・スタインマン氏が発見した細胞です。スタインマン氏は4年前に膵臓がんを患い、樹状細胞を使った免疫療法により延命していたそうですが、受賞直前に亡くなりました。まだまだ時間がかかりそうです。
今後は、イピリムマブなどを中心として、他の免疫療法や分子標的薬あるいは化学療法役を組み合わせて、抗がん効果の増強を狙うことになると思います。



コメント