人類に希望をもたらす2023年の医学的ブレイクスルー7選…ノーベル賞技術による遺伝子治療から両親ともオスのマウス、膵臓がんの予測技術まで
以下は、記事の抜粋です。
新型コロナウイルス感染症は2023年も人々の命を奪い続け、全世界の累計死者数は700万人近くに達した。長い後遺症に苦しむ人々も大勢いる。しかし、2023年は悪いニュースばかりではなかった。
このウイルスに対する免疫を獲得した人々の割合が高まったため、WHOは5月5日に、新型コロナはもはや「国際的に懸念される公衆衛生上の緊急事態(PHEIC)」ではないと決定した。新しい変異株に対応したワクチンが使われるようになったことで、感染者数、入院者数、死者数が減少した。
2023年には、新型コロナワクチンのほかにも多くの興味深い画期的な発見がなされた。なかでも私たちの健康と医療に大きな影響を与えそうな発見は特に注目に値する。
1. ゲノム編集技術「CRISPR」による世界初の遺伝子治療が可能に
ゲノム編集技術「CRISPR(クリスパー)」に基づく世界初の遺伝子治療が、英国と米国の医薬品規制当局によって承認された。対象となるのは、鎌状赤血球症とβサラセミアという遺伝子疾患だ。いずれも赤血球内のヘモグロビンというタンパク質に影響を及ぼし、貧血などの症状が現れる。
新たに承認された遺伝子治療は「CASGEVY」と呼ばれ、患者の造血幹細胞内の異常なヘモグロビン遺伝子を修正し、正常に機能するヘモグロビンを作れるようにする。患者の骨髄から幹細胞を採取し、実験室で編集した後、再び患者に注入する。1回の遺伝子治療で治る人もいるかもしれないと期待されている。
現在、ほかの遺伝病や、がん、不妊症など、多数の病気についてクリスパーを用いた治療法の開発が進んでいる。
2. アルツハイマー病の進行を遅らせる最初の薬が承認される
米食品医薬品局(FDA)や日本の厚生労働省は、アルツハイマー病の原因とされるものを標的とする初の治療薬「レカネマブ(商品名レケンビ)」を承認した。
この薬は、アルツハイマー病を完治させるものでも、末期のアルツハイマー病の症状を改善するものでもない。だが、初期に投与すれば、治療開始から18カ月後の認知機能の低下が、プラセボを投与された患者に比べて27%少ないことが臨床試験で示されている。
レケンビは、アルツハイマー病の特徴である脳内のアミロイド斑を標的とするモノクローナル抗体だ。アミロイド斑の蓄積は記憶力や思考力を低下させ、アルツハイマー病の原因となると考えられている。臨床試験では、レケンビが脳内のアミロイド斑を除去し、病気の進行を遅らせることが示されている。
3. 2匹のオスのマウスからメスの卵子なしで健康な子どもを作る
大阪大学の林克彦氏ら日本の研究チームが、メスのマウスの卵子なしで、健康で繁殖能力のあるマウスを生み出せることを示し、国際学会で発表した。彼らはまず、オスのマウスの皮膚細胞に由来する幹細胞から卵子を作った。この卵子を別のオスの精子によって受精させ、受精卵をメスのマウスに移植して成長・成熟させた。
移植された600個以上の胚のうち、子どものマウスに成長したのは7個だけだったが、子どもたちは正常に成長し、成体になると繁殖能力を示した。ただし、このマウスの子どもたちが、従来の交配で生まれた子どもたちと完全に同じように発育するかどうかはまだわかっていない。
4. 昆虫の脳のすべての結合をマッピング
科学者たちが、昆虫の脳の完全な配線図を初めて作り上げた。たいした成果ではないように思われるかもしれないが、相互に接続されたニューロンのネットワーク全体(コネクトーム)は、ショウジョウバエの脳であっても膨大だ。これまでに完全な配線図が作成されているのは、線虫、ホヤ、ゴカイの脳だけで、いずれも結合の数は数百程度だった。
しかし、ショウジョウバエの幼虫のコネクトームともなると、ニューロンの数は3000以上、ニューロン間の結合の数は50万以上もある。国際的な科学者チームによる配線図の作成には、5年以上の歳月を要した。ショウジョウバエの脳は人間の脳よりはるかに単純だが、今回開発された技術は、将来、より複雑な脳のマッピングに役立つはずだ。
ショウジョウバエの脳のコネクトームを理解することは、ヒトの脳の働きや神経疾患の発症メカニズムの解明に役立つだけでなく、新しい機械学習手法や、より効率的な人工知能(AI)システムの開発にもつながることが期待される。
5. 髪の色を作る細胞が動けなくなると白髪になると発見
科学者たちは、色素を作る「メラノサイト」という細胞が未熟な状態のまま動けなくなると、金、茶、赤、黒などの髪色を作れなくなることを示した。
新しい毛髪は皮膚内の毛包から成長し、毛包にはメラノサイトも存在している。ニューヨーク大学の伊藤真由美氏らは、マウスの毛包の中でメラノサイト幹細胞が上下に移動する様子を2年間にわたり観察した。
意外なことに、メラノサイト幹細胞は、毛髪のライフサイクルを通じて毛包の中を上下に移動しながら、未熟な幹細胞の状態と色素を作る成熟したメラノサイトの状態を行ったり来たりしていた。しかし、毛髪が老化するとメラノサイト幹細胞の動きが遅くなり、ついには未熟な状態のまま毛髪の根元付近で動けなくなってしまう。こうして色素が作られなくなると、髪は白くなる。
6. がんの進行や転移を助ける細菌
科学者たちは、がん細胞が体の免疫反応から逃れるのを、多くの消化管のがんでよく見られる一部の細菌が直接助けていることを発見した。これらの細菌はさらに、がん細胞と協力してがんの進行を促すだけでなく、抗がん剤を分解したり、抗がん剤への抵抗性を持たせたりして、がん細胞の転移を速めている。
この研究は、がんの中にすみ着いている細菌も殺すことで効果を発揮する抗がん剤があることを示唆している。がんの微小環境が、がんの生存と進行にどのように影響するかを理解できれば、がん治療に新たな扉を開くことになる。
7. 膵臓がんリスクの高い人をAIで発見
患者の医療記録に現れるパターンから、実際の診断の3年も前に膵臓がんを予測しうる新しいAIツールが発表された。
膵臓がんは比較的まれながんだが、部位別のがんによる死亡数では、米国では肺、大腸に次ぐ第3位、日本では肺、大腸、胃に次ぐ第4位を占めている。膵臓がんが恐ろしいのは、発見されるときにはすでに末期で、ほかの部位に広がっていることが多いからだ。
早期の段階で発見できれば、多くの患者はもっと長く生きられる。そこで科学者たちは、デンマークの約620万人について41年分の医療記録をAIアルゴリズムに学習させ、のちに膵臓がんと診断された約2万4000人の患者の記録に隠されたパターンを検出した。
医療記録には、それぞれの病名がコードで記録されている。AIモデルは、これらの疾患コードと発生時期の組み合わせを分析した。膵臓がんと診断される前の一連の病態を比べて、AIモデルは膵臓がんのリスクが最も高い患者を特定できるようになった。
科学者たちは次に、21年にわたる約300万人の米国退役軍人の記録を分析し、このAIツールをテストした。するとコンピューターアルゴリズムは、膵臓がんになった約4000人を、実際に診断される3年前までに正しく識別することができた。
良く勉強しているつもりでしたが、半分以上知りませんでした。
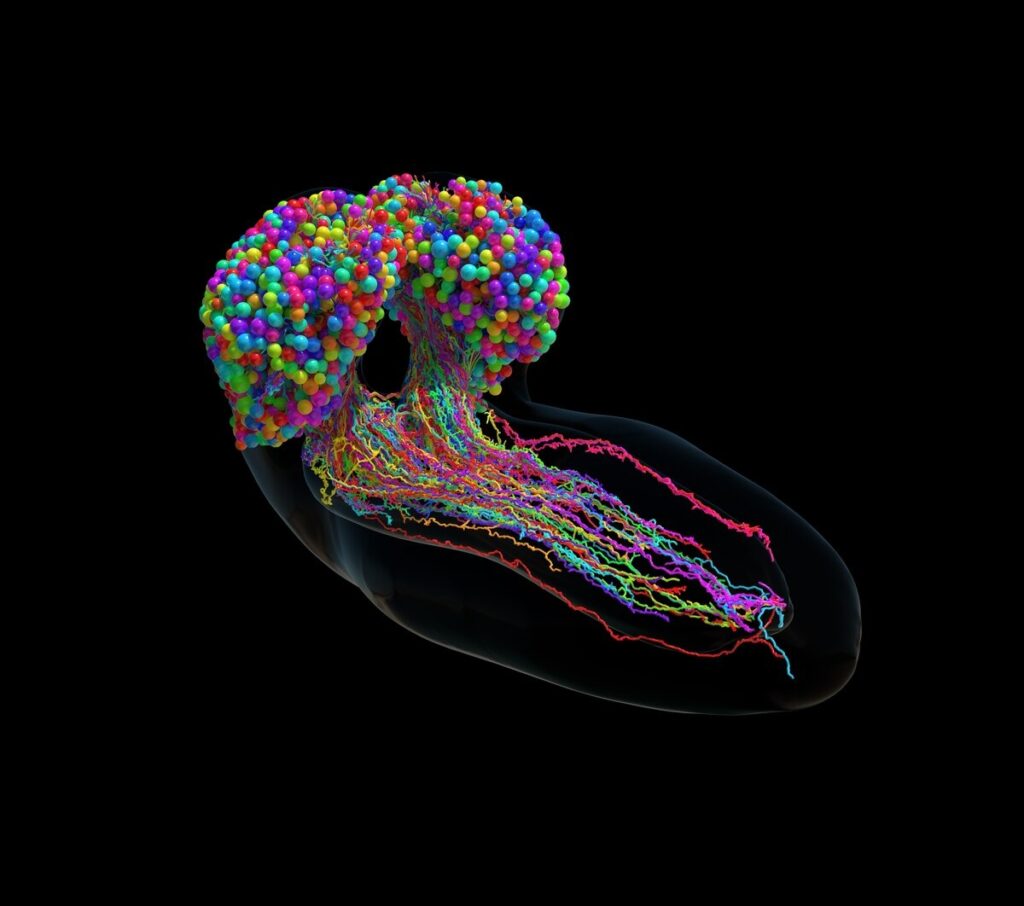
ショウジョウバエの幼虫の中枢神経系における分化したニューロンの形と構造を示したもの。



コメント