熱ショックタンパク90阻害薬ピミテスピブ(pimitespib) 、消化管間質腫瘍(GIST)に承認
以下は、記事の抜粋です。
大鵬薬品は 2022年6月20日、経口HSP(Heat Shock Protein)90阻害薬ピミテスピブ(pimitespib、製品名:ジェセリ)について、「がん化学療法後に増悪した消化管間質腫瘍」の効能・効果での製造販売承認取得を発表した。
同剤は、大鵬薬品が創製した化合物で、HSP90を阻害することによりがんの増殖や生存などに関与するKIT、PDGFRA、HER2やEGFRなどのタンパクを不安定化し、減少させることで抗腫瘍効果を示す。
今回の承認は、標準治療薬に不応または不耐と判断されたGIST患者を対象に、同剤とプラセボの有効性および安全性を比較した第III相臨床試験(CHAPTER-GIST-301試験)の結果に基づいたものである。同試験においてpimitespibは主要評価項目の無増悪生存期間(PFS)を有意に延長し、有害事象は管理可能であった。
HSP90は、主要な細胞内分子シャペロンの一つで、細胞ストレス状況下で発現量が増大する細胞質に多く存在するタンパク質です。HSP90は、プロテインキナーゼやステロイドホルモン受容体等の細胞増殖や分化に重要な役割を果たすシグナル伝達分子などの様々なタンパク質と相互作用してその機能を保証します。これまでも、ゲルダナマイシンというHSP90阻害薬で培養癌細胞の増殖が抑制され、実験動物での腫瘍縮小効果が報告されていましたが、臨床的に有用なHSP90阻害薬はありませんでした。
ピミテスピブは、これまでに開発された最も選択的な HSP90α および β 阻害剤の 1 つで、相同性の高い HSP90 ファミリーメンバーである GRP94 および TRAP1 よりも、HSP90α および β に対してより高い特異的結合を示すそうです。おそらく、HSP90α および βに依存して働いている細胞内のがん化因子の働きを抑制しているのだと思います。
第III相臨床試験(CHAPTER-GIST-301試験)での無増悪生存期間の中央値は、ピミテスピブで 2.8 か月、プラセボで 1.4 か月 [ハザード比 (HR) 0.51 ]。最も一般的 (≥30%) の治療関連の有害事象 は、下痢 (74.1%) と食欲減退 (31.0%) でした(論文をみる)。
今後もHSP90を標的とした新薬は出てくる可能性があると思います。今後の発展に期待します。
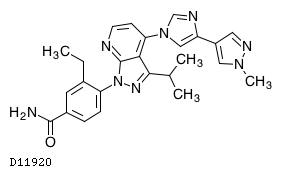
ピミテスピブの構造


コメント